(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为___________ 。
题目
(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为___________ 。
相似考题
参考答案和解析
Na2O+2CO2+H2O=2NaHCO3
更多“(2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为___________。 ”相关问题
-
第1题:
红磷燃烧除需要氧气外,还需满足的条件是_______________;该反应
的化学方程式为_________________;用红磷做“测定空气里氧气含量”的
实验时,若红磷的量不足,所测得氧气的体积分数_____________(填“偏大"、“偏小"或“不变”)。
正确答案:
-
第2题:
(8分)
汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物有:CmHn(烃)、SO2、NOX、CO和C等,请回答下列有关问题。
(1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为 ,汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由 能转化为 能,最终转化为机械能;
(2)通过车用燃油的精炼加工处理,可减少汽车尾气中的 (填化学式,多填本空不得分)排放;
(3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下NOX与CO反应的化学方程式 。
正确答案: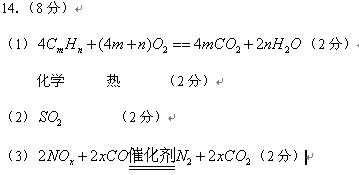
-
第3题:
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_____。
正确答案: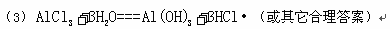
-
第4题:
水与金属钾反应的化学方程式为2K+2H2O=2KOH+H2↑。
此题为判断题(对,错)。
正确答案:√
-
第5题:
颗粒大小达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”。
⑴在高温条件下,用H2与FeCl2反应,可生成“纳米铁”和一种溶于水显强酸性的气体,写出该反应的化学方程式( ) 。
⑵“纳米铁”在空气中受撞击时会燃烧,其反应与铁在纯氧中燃烧相同,写出该反应的化学方程式( ) 。
⑶请你预测“纳米铁”的其他化学性质,用化学反应方程式表示( ) 。答案:解析:
-
第6题:
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: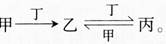
下列有关物质的推断不正确的是( )。
A.若甲为Fe,则丁可能是Cl2
B.若甲为焦炭,则丁可能是O2
C.若甲为SO2,则丁可能是NaOH溶液
D.若甲为AlCl3溶液,则丁可能是NaOH溶液答案:A解析: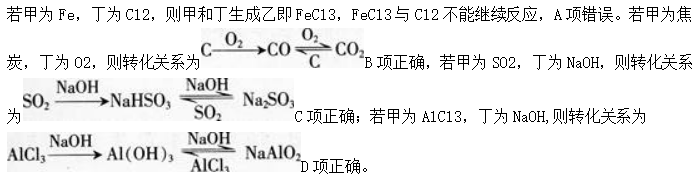
-
第7题:
某同学研究硫酸亚铁受热分解反应时,作了两种假设: (1)假设它按KClO3受热分解方式来分解,则化学方程式是(), (2)假设它按CaCO3受热分解方式来分解,则化学方程式是()。事实上由于FeO易被氧化,FeSO4的分解产物是Fe2O3、SO2、SO3,分解温度为500℃左右,则化学方程式是()
正确答案:FeSO4===FeS+2O2;FeSO4===FeO+SO3;2FeSO4===Fe2O3+SO2+SO3 -
第8题:
变换反应的化学方程式为()。
正确答案:CO+H2O(g)=H2+CO2 -
第9题:
甲、乙、丙、丁4种物质均为只含有两种元素的化合物,其分子中均含有18个电子,下列说法中正确的是()。
- A、若气体甲的水溶液在常温下的pH<7,则甲一定为HCl
- B、若乙的摩尔质量与O2相同,则乙一定为N2H4
- C、若3.0g丙的物质的量为0.1mol,则丙一定为甲烷的同系物
- D、若丁为四原子分子.则丁一定能使品红溶液褪色
正确答案:C -
第10题:
若反应2NO+Cl2===2NOCl是基元反应,则该反应的反应速度方程式可写为(),反应是()级反应。
正确答案:v=kc(NO)2 c(Cl2);3 -
第11题:
填空题某同学研究硫酸亚铁受热分解反应时,作了两种假设: (1)假设它按KClO3受热分解方式来分解,则化学方程式是(), (2)假设它按CaCO3受热分解方式来分解,则化学方程式是()。事实上由于FeO易被氧化,FeSO4的分解产物是Fe2O3、SO2、SO3,分解温度为500℃左右,则化学方程式是()正确答案: FeSO4===FeS+2O2,FeSO4===FeO+SO3,2FeSO4===Fe2O3+SO2+SO3解析: 暂无解析 -
第12题:
单选题根据化学方程式2H2+O2=2H2O,若已知参加反应的O2为32g,H2前面的计量数表示( ).A分子数
B物质的量数
C质量数
D体积数
正确答案: D解析:
32g氧气的物质的量为1mol,因此该反应消耗氢气的物质的量为2mol,即H2前面的计量数表示物质的量数. -
第13题:
反应①的化学方程式为: ______________
正确答案: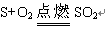
-
第14题:
(2)A与C反应的化学方程式:________________。
正确答案: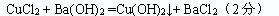
-
第15题:
选择氧气,一氧化碳或二氧化碳填空,并写出有关反应的化学方程式:
(1)能使带火星的木条复燃的是_______________;
(2)能用于灭火的是______________;
(3)属于有毒气体的是___________;
(4)绿色植物进行光合作用吸收的是___________,释放的是_________;
(5)能在空气中燃烧的是________,反应的化学方程式是_________________:
选择氧气,一氧化碳或二氧化碳填空,并写出有关反应的化学方程式:
(6)能使澄清石灰水变浑浊的是________,反应的化学方程式是_________________;
(7)能使紫色石蕊试液变成红色的是________,它与水反应的化学方程式是________
__________________;
(8)能使氧化铜还原成铜的是_____________,反应的化学方程式是_________________
________________________;
(9)干冰是___________________。
(1)氧气 (2)二氧化碳 (3)一氧化碳 (4)二氧化碳 氧气 (5)一氧化碳 2CO+O2 点燃 2CO2 (6)二氧化碳 CO2+Ca(OH)2=CaCO3↓+H2O (7)二氧化碳 CO2+H2O=H2CO3 (8)一氧化碳 CuO +CO = Cu+ CO2 (9)固态二氧化碳 -
第16题:
②B与新制的Cu(OH)2反应生成D,其化学方程式为______________.
正确答案:
-
第17题:
右图中的物质都是初中化学常见物质,其中A、B为单质,B是可供动植物呼吸的气体;甲、乙、丙为化合物,甲与过量的丙、乙与过量的丙两两反应的所有产物相同。图中“—”表示两端的物之间能发生化学反应;“→”表 示物质间存在转化关 系;部分反应物或生成物已略去。
(1)写出B的化学式___________________;写出一种丙的名称___________________。
(2)写出A和甲反应的化学方程式:___________________。
(3)写出乙→甲的化学方程式:___________________。答案:解析:(1)O2 氢氧化钠(或氢氧化钙等) (2)C+CO2====2CO (3)H2CO3=CO2↑+H2O -
第18题:
钠离子交换软化过程中,碳酸氢盐硬度的交换反应式为()和()。
正确答案:Ca(HCO3)2+2NaR=CaR2+2NaHCO3;Mg(HCO3)2+2NaR=MgR2+2NaHCO3 -
第19题:
金属M与AgNO3溶液反应的化学方程式为M+2AgNO3===M(NO3)2+2Ag。则下列说法错误的是()
- A、M的金属活动性比Ag强
- B、金属M可能是铜
- C、该反应属于复分解反应
- D、该反应前后M的化合价发生了改变
正确答案:C -
第20题:
若某反应的反应速率常数的单位为dm6·mol-2-2·s-1,则该反应的级数为()
正确答案:3 -
第21题:
将热量Q传给一定量的理想气体, (1)若气体的体积不变,则其热量转化为(); (2)若气体的温度不变,则其热量转化为(); (3)若气体的压强不变,则其热量转化为()。
正确答案:气体内能;气体对外做功;内能和对外做功 -
第22题:
某反应物在一定时间内完全转化为产物,则反应的级数为()。
- A、0
- B、1
- C、2
- D、3
正确答案:A -
第23题:
填空题氨合成反应的化学方程式为()、反应特点是:()、()、(),其反应速率(),只有在()作用下反应才有较快速度。正确答案: 1/2N2+3/2H2==NH3(g),放热,体积减小,可逆反应,较慢,催化剂解析: 暂无解析
