单选题29号元素的核外电子分布式为( )。[2011年真题]A 1s22s22p63s23p63d94s2B 1s22s22p63s23p63d104s1C 1s22s22p63s23p64s13d10D 1s22s22p63s23p64s23d9
题目
1s22s22p63s23p63d94s2
1s22s22p63s23p63d104s1
1s22s22p63s23p64s13d10
1s22s22p63s23p64s23d9
相似考题
更多“29号元素的核外电子分布式为( )。[2011年真题]”相关问题
-
第1题:
某元素原子的核外电子排布为1S22S22P63S1,该元素的原子序数为(),核内质子数为(),元素符号为()。参考答案: ll;l1;Na
-
第2题:
某元素原子的核外电子排布为1S22S22P63S1,该元素的原子序数为l1,核内质子数为11 ,元素符号为( )
正确答案:Na
-
第3题:
铝(第13号元素)的核外电子排布式的正确表达式为( )。A.
B.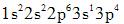
C.
D. 答案:C解析:核外电子分布情况遵循三项基本原则:①能量最低原理;②泡利不相容原理;③洪特规则。根据铝元素核外共容纳13个电子,s轨道最多可容纳2个电子,p轨道最多可容纳6个电子。
答案:C解析:核外电子分布情况遵循三项基本原则:①能量最低原理;②泡利不相容原理;③洪特规则。根据铝元素核外共容纳13个电子,s轨道最多可容纳2个电子,p轨道最多可容纳6个电子。 -
第4题:
下列元素原子的核外电子分布式正确的是( )。A.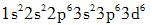
B.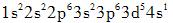
C.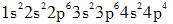
D.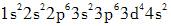 答案:B解析:核外电子的分布要依据原子轨道的近似能级顺序和核外电子排布的规则。原子轨道的近似能级顺序为1s,2s、2p,3s、3p,4s、3d、4p,5s、4d、5p,6s、4f、5d、6p,7s、5f、6d、7p。核外电子排布从最内层到外层依次为2,8,8,18,18,32…2n2(n为电子层数)。
答案:B解析:核外电子的分布要依据原子轨道的近似能级顺序和核外电子排布的规则。原子轨道的近似能级顺序为1s,2s、2p,3s、3p,4s、3d、4p,5s、4d、5p,6s、4f、5d、6p,7s、5f、6d、7p。核外电子排布从最内层到外层依次为2,8,8,18,18,32…2n2(n为电子层数)。 -
第5题:
互为同位素的元素,其特性是()。
- A、核外电子数与中子数相同
- B、核外电子数与质子数相同
- C、核外电子数相同,核内中子数不同
- D、核外电子数等于中子和质子之和
- E、核外电子数等于中子与质子之差
正确答案:C -
第6题:
元素的性质主要决定于核外电子的排布,特别是()的排布。
正确答案:最外层电子 -
第7题:
已知某元素+2价离子的核外电子排布式为:[Ar]3d5,该元素在周期表中处于()周期、()族、()区,元素符号是()。
正确答案:第四;ⅦB;d;Mn -
第8题:
请描述碳元素的核外电子轨道形状和电子分布情况。为什么说在生命元素中,碳元素具有特别重要的作用?
正确答案: C.原子的最外层电子有4个,其基态分别处在2s(两个)和2P(两个)轨道上,当C原子发生反应时,首先一个2S电子被激发到2P轨道上,然后由一个2S电子轨道和3个2P轨道发生杂化,形成4个完全一样的SP3轨道.其立体形状就像一个正四面体,4个轨道伸向4面,各轨道间的夹角都是109°28′’。C原子采用SP3杂化方式来反应有助于生成更稳定的键。在生命元素中,碳元素具有特别重要的作用,碳原子相互连接成链或环,形成各种生物大分子的基本结构。
除了水以外,含碳化合物是生物体中最普遍的物质。由细胞合成的含碳化合物是有机化合物或生物分子。碳原子之间即与其他原子间以共价键等形式相结合,可以形成大量化学性状与相对分子质量不同的生物分子。碳原子是生物大分子的基本骨架:碳原子的不同排列方式和长短是生物大分子多样性的基础。所有生物大分子都是以碳原子相互连接成链或成环作为基本结构,并以共价键的形式与氢、氧、氮及磷相结合,形成了具有不同性质的生物大分子。 -
第9题:
原子序数为17的元素,其原子核外电子排布式为();未成对电子数为1。
正确答案:1s22s22p63s23p5 -
第10题:
导电性最佳的金属Ag(填元素符号);其外层电子分布式为()。
正确答案:4d105s1 -
第11题:
单选题某原子序数为15的元素,其基态原子的核外电子分布中,未成对电子数是( )。[2017年真题]A0
B1
C2
D3
正确答案: B解析:
正确书写核外电子分布式,可先根据三个分布规则和近似能级顺序将电子依次填入相应轨道,再按电子层顺序整理一下分布式,按n由小到大自左向右排列各原子轨道,相同电子层的轨道排在一起。原子序数为15的元素基态原子的核外电子分布为:1s22s22p63s23p3,未成对电子数是3。 -
第12题:
单选题互为同位素的元素,3其特性是()A核外电子数与中子数相同
B核外电子数与质子数相同
C核外电子数相同,核内中子数不同
D核外电子数等于中子和质子之和
E核外电子数等于中子与质子之差
正确答案: C解析: 暂无解析 -
第13题:
元素R的原子质量数为35,中子数为18,核外电子数是( )。
A.16
B.19
C.17
D.18
正确答案:C
-
第14题:
29号元素的核外电子分布式是( )。A.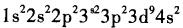
B.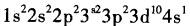
C.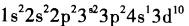
D.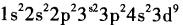 答案:B解析:按照原子核外电子排布规律,29号铜元素位于元素周期表第四周期IB,符合全满比较稳定的特例,应为B。
答案:B解析:按照原子核外电子排布规律,29号铜元素位于元素周期表第四周期IB,符合全满比较稳定的特例,应为B。 -
第15题:
29号元素的核外电子分布式为: 答案:B解析:根据原子核外电子排布三大原则排布核外电子。
答案:B解析:根据原子核外电子排布三大原则排布核外电子。 -
第16题:
29号元素的核外电子分布式是( )。 答案:B解析:提示:按照原子核外电子排布规律,29号铜元素位于元素周期表第四周期IB,符合全满比较稳定的特例,应为B。
答案:B解析:提示:按照原子核外电子排布规律,29号铜元素位于元素周期表第四周期IB,符合全满比较稳定的特例,应为B。 -
第17题:
某元素最高正价与负价绝对值之差为4,该元素的离子与跟其核外电子排列相同的离子形成的化合物是()
- A、K2S
- B、MgO
- C、MgS
- D、NaF
正确答案:A -
第18题:
某元素的原子核外有三层电子层,最外层电子数是核外电子数的1/6,该元素的元素符号是Mg。
正确答案:正确 -
第19题:
通过元素周期表,可以知道元素的()。
- A、符号
- B、原子量
- C、电子数
- D、核外电子排布
正确答案:A,B,C -
第20题:
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。
正确答案:⑴A:1s22s22p63s23p63d24s2;B:1s22s22p63s23p63d104s24p3。
⑵A:第四周期ⅣB族;B:第四周期ⅤA族。 -
第21题:
某元素原子主量子数n为4的电子层上有7个电子,该元素原子外层电子构型是(),未成对电子数为(),原子核外电子分布式为(),该元素原子序数是(),它位于第()周期,第()族,最高氧化数()。
正确答案:4s24p5;1;1s22s22p63s23p63d104s24p5;35;四;ⅦA;+7 -
第22题:
氢是新型清洁能源,但难储运。研究发现,镧和镍的一种合金是储氢材料。下列有关57号元素镧(La)的说法不正确的是()
- A、该元素原子的质子数为57
- B、该元素原子的核电荷数为57
- C、该元素原子的核外电子数为57
- D、该元素为非金属元素
正确答案:D -
第23题:
单选题29号元素的核外电子分布式为( )。[2011年真题]A1s22s22p63s23p63d94s2
B1s22s22p63s23p63d104s1
C1s22s22p63s23p64s13d10
D1s22s22p63s23p64s23d9
正确答案: C解析:
29号元素为铜,核外电子数为29,按照能量最低原理,电子分布式应为1s22s22p63s23p64s23d9。根据洪特规则,3d10为全充满稳定,因此4s轨道的一个电子调整到3d;又由于屏蔽效应导致4s轨道电子受原子核的吸引力减小,轨道能量升高,所以填充满电子之后,3d轨道的能量比4s轨道能量低。因此最终电子分布式为1s22s22p63s23p63d104s1。 -
第24题:
问答题请描述碳元素的核外电子轨道形状和电子分布情况。为什么说在生命元素中,碳元素具有特别重要的作用?正确答案: C.原子的最外层电子有4个,其基态分别处在2s(两个)和2P(两个)轨道上,当C原子发生反应时,首先一个2S电子被激发到2P轨道上,然后由一个2S电子轨道和3个2P轨道发生杂化,形成4个完全一样的SP3轨道.其立体形状就像一个正四面体,4个轨道伸向4面,各轨道间的夹角都是109°28′’。C原子采用SP3杂化方式来反应有助于生成更稳定的键。在生命元素中,碳元素具有特别重要的作用,碳原子相互连接成链或环,形成各种生物大分子的基本结构。
除了水以外,含碳化合物是生物体中最普遍的物质。由细胞合成的含碳化合物是有机化合物或生物分子。碳原子之间即与其他原子间以共价键等形式相结合,可以形成大量化学性状与相对分子质量不同的生物分子。碳原子是生物大分子的基本骨架:碳原子的不同排列方式和长短是生物大分子多样性的基础。所有生物大分子都是以碳原子相互连接成链或成环作为基本结构,并以共价键的形式与氢、氧、氮及磷相结合,形成了具有不同性质的生物大分子。解析: 暂无解析
