已知Ka(HAc)大于Ka(HCN),所以CN是比Ac强的碱。
题目
已知Ka(HAc)大于Ka(HCN),所以CN是比Ac强的碱。
相似考题
参考答案和解析
更多“已知Ka(HAc)大于Ka(HCN),所以CN是比Ac强的碱。”相关问题
-
第1题:
某生物碱的碱性强,那么其
A、pKa小
B、pKa大
C、Ka大
D、Ka小
E、以上都不对
参考答案:B
-
第2题:
某生物碱的碱性强,则其A. pKA. 小
B. pKB. 大
C. KA. 大
D. pKA. 大
E. KA. 小答案:D解析:生物碱碱性强弱用pKa表示,pKa越大,碱性越强。 -
第3题:
配制pH=7的缓冲溶液时,选择最合适的缓冲对是()。[Ka(HAc)=1.8×10-5,Kb(NH3)=1.8×10-5,H2CO3Ka1=4.2×10-7,Ka2=5.6×10-11,H3PO4Ka1=7.6×10-3,Ka2=6.3×10-8,Ka3=4.4×10-13]()
- A、HAc–NaAc
- B、NH3–NH4Cl
- C、NaH2PO4–Na2HPO4
- D、NaHCO3–Na2CO3
正确答案:C -
第4题:
浓度为c的弱酸能够用标准碱直接滴定的条件是()
- A、c·Ka≥10-4
- B、c·Ka≥10-8
- C、c·Ka≥10-6
- D、c·Ka≥10-5
正确答案:B -
第5题:
向HAc溶液中加入NaAc固体时,HAc的Ka()
- A、增大
- B、不变
- C、减小
- D、先增大后减小
正确答案:A -
第6题:
HAc的Ka=1.76×10-5,欲配制pH=4.50的缓冲溶液,若用HAc及NaAc配制,则二者的浓度比cNaAc/cHAc为()。
- A、等于1
- B、大于1
- C、大于2
- D、小于1
正确答案:D -
第7题:
HAc-NaAc缓冲溶液的计算公式为()。
- A、[H+]=KaC酸/C盐
- B、[H+]=C·Ka
- C、[H+]=Ka1·Ka2
正确答案:A -
第8题:
已知HAc的Ka=1.7×10-5、HCN的Ka=6.2×10-10,其酸的强度()大于();而相应共轭碱的强度()大于()。
- A、Ac-;HAc;HCN;CN-
- B、CN-;Ac-;HAc;HCN
- C、HCN;CN-;Ac-;HAc
- D、HAc;HCN;CN-;Ac-
正确答案:D -
第9题:
根据下列质子传递反应 (1)HS-+H2O=S2- + H3O+ K1=1×10-12 (2)CN-+ H3O = HCN+H2O K2= 1×10-4 (3)HAc +H2O=H3O++Ac- K3=1×10-5 (4)HNO2+CN-=HCN+NO2-K4=1×106 最强的质子碱是()
- A、NO2-
- B、Ac-
- C、CN-
- D、S2-
正确答案:D -
第10题:
已知Ka(HAc)为1.8×10-5,若用HAc和NaAc配制成pH=5的缓冲溶液,则HAc的浓度与NaAc的浓度之比正确的为()。
- A、8:9
- B、9:8
- C、5:9
- D、9:5
正确答案:C -
第11题:
判断题已知Ka(HAc)大于Ka(HCN),所以CN是比Ac强的碱。A对
B错
正确答案: 错解析: 暂无解析 -
第12题:
单选题已知HCl和HAc的水溶液Ka值分别为Ka≥1和Ka=1.7×10-5,产生这种差别的原因是()A容积的拉平效应
B酸效应
C盐效应
D溶剂的区分效应
正确答案: A解析: 暂无解析 -
第13题:
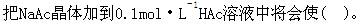 A.溶液的pH值降低
A.溶液的pH值降低
B.Ka,HAc增加
C.溶液的pH值升高
D.Ka,HAc减小答案:C解析:
-
第14题:
有一混合酸溶液,其中HF的浓度为1.0mol/L,HAc的浓度为0.10mol/L,求溶液中H+,F-,Ac-,HF和HAc的浓度已知:Ka(HF)=3.53×10-4 Ka(HAc)=1.76×10-5
正确答案: [H+]=0.0188(M)
[F-]=0.0188(M)
[Ac-]=9.36×10-5(M)
[HF]=0.98(M)
[HAc]=0.1(M) -
第15题:
已知HCl和HAc的水溶液Ka值分别为Ka≥1和Ka=1.7×10-5,产生这种差别的原因是()
- A、容积的拉平效应
- B、酸效应
- C、盐效应
- D、溶剂的区分效应
正确答案:D -
第16题:
一元弱酸HB的电离常数Ka(HB)与其共轭碱B的电离常数Kb(B‾)在水溶液中的关系是()。(Kw=Ka*Kb)
- A、Ka(HB)=Kb(B‾)
- B、Ka(HB)Kb(B‾)=1
- C、Ka(HB)Kb(B‾)=Kw
- D、Ka(HB)/Kb(B‾)=Kw
正确答案:C -
第17题:
欲配制pH=4.6和pH=7.0的缓冲溶液,应先用()(已知:KaΘ(HCOOH)=1.8×10–4,KaΘ(HAc)=1.8×10–5,KbΘ(NH3)=1.8×10–5,H2CO3的Ka2Θ=5×10–11,H3PO4的Ka2Θ=1.0×10–7)
- A、HCOOH—HCOONa和NaHCO3—Na2CO3
- B、HAc—NaAc和NaH2PO4—NaHPO4
- C、HCOOH—HCOONa和NH3—NH4Cl
- D、HAc—NaAc和NH3—NH4Cl
正确答案:B -
第18题:
HAc(Ka=1.8×10-5),HCOOH(Ka=1.8×10-4),H2C2O4(Ka=5.9×10-2),氯乙酸(Ka=1.4×10-3)则最强酸是()。
- A、HAc
- B、氯乙酸
- C、H2C2O4
- D、HCOOH
正确答案:C -
第19题:
0.1mol/L的下列溶液中,酸性最强的是()。
- A、H3BO3(Ka=5.8×10-10)
- B、NH3•H2O(Kb=1.8×10-5)
- C、苯酚(Ka=1.1×10-10)
- D、HAC(Ka=1.8×10-5)
正确答案:D -
第20题:
电流单位大于安培的有()。
- A、μA
- B、A
- C、mA
- D、kA
正确答案:D -
第21题:
水、HAc、HCN的共轭碱的碱性强弱的顺序是:()
- A、OH->Ac->CN-
- B、CN->OH->Ac-
- C、OH->CN->Ac-
- D、CN->Ac->OH-
正确答案:C -
第22题:
单选题已知HAc的Ka=1.7×10-5、HCN的Ka=6.2×10-10,其酸的强度()大于();而相应共轭碱的强度()大于()。AAc-;HAc;HCN;CN-
BCN-;Ac-;HAc;HCN
CHCN;CN-;Ac-;HAc
DHAc;HCN;CN-;Ac-
正确答案: D解析: 暂无解析 -
第23题:
单选题浓度为c的弱酸能够用标准碱直接滴定的条件是()Ac·Ka≥10-4
Bc·Ka≥10-8
Cc·Ka≥10-6
Dc·Ka≥10-5
正确答案: A解析: 暂无解析
