用盐酸清洗玻璃电极上沾有的胶质,盐酸溶液的浓度应为()mol/L。A、2B、0.2C、1D、0.1
题目
用盐酸清洗玻璃电极上沾有的胶质,盐酸溶液的浓度应为()mol/L。
- A、2
- B、0.2
- C、1
- D、0.1
相似考题
更多“用盐酸清洗玻璃电极上沾有的胶质,盐酸溶液的浓度应为()mol/L。A、2B、0.2C、1D、0.1”相关问题
-
第1题:
用盐酸清洗玻璃电极上沾有的无机盐类,盐酸溶液的浓度应为()mol/L。A、2
B、0.2
C、1
D、0.1
参考答案:D
-
第2题:
盐酸溶液的标定:取干燥至恒重的基准无水碳酸钠0.1502g,加水50ml使溶解,依法标定,消耗0.1mol/L盐酸滴定液28.28ml,已知每1ml盐酸滴定液(0.1mol/L)相当于5.30mg的无水碳酸钠,示盐酸滴定液的浓度为
A.0.9979(mol/L)
B.0.100(mol/L)
C.1.002M
D.0.1002(mol/L)
E.0.1002M
正确答案:D
-
第3题:
新玻璃器皿清洗应先用下列溶液浸泡的是
A、2%盐酸
B、肥皂水
C、洗涤剂溶液
D、洗衣粉溶液
E、0.1mol/LNaOH
参考答案:A
-
第4题:
将6 mL 0.2 mol/L盐酸与10 mL 0.1 mol/L氨水混合,完全反应后,溶液中各种离子浓度的相对大小是.答案:解析: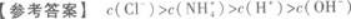 【解题指要】(1)首先要强调,将两种溶液混合时必须考虑这一过程中是否发生化学反应.如本题是将盐酸与氨水混合,会发生化学反应:
【解题指要】(1)首先要强调,将两种溶液混合时必须考虑这一过程中是否发生化学反应.如本题是将盐酸与氨水混合,会发生化学反应:

根据HCl和NH3的数量的不同.可能有三种情况:
①恰好完全反应,此时就变成NH4Cl溶液;
②HCl有剩余,此时就是NH4Cl和HCl的混合溶液;
③NH3有剩余,此时就是NH4Cl与NH3的混合溶液.
(2)盐酸中HCl的物质的量为:0.2 mol/L×0.006 L=0.001 2 mol.
氨水中NH3的物质的量为:0.1 mol/L×0.01 L=0.001 mol.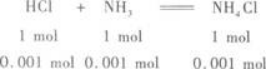
所以,反应后生成NH4Cl 0.001 mol,剩余的HCl为0.001 2 mol-0.001 mol=0.000 2 mol.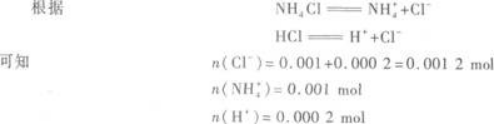
以上物质的量的大小顺序就是离子浓度的大小顺序.
另外,一般情况下,溶液均指水溶液,所以溶液中还有水电离出来的H+和OH-两种离子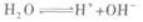
此题中酸有剩余,所以c(H+)一定大于c(OH-).
-
第5题:
最常见的玻璃膜电极为pH玻璃电极,它的敏感膜由特殊成分的玻璃制成的厚约0.05mm的玻璃球,球内盛有的内参比溶液为A.1.0mol/L HCl溶液
B.0.02mol/L HCl溶液
C.0.1mol/L NH Cl溶液
Cl溶液
D.0.2mol/L HCl溶液
E.0.1mol/L HCl溶液答案:E解析:常见的玻璃膜电极为pH玻璃电极,它的敏感膜由特殊成分的玻璃制成的厚约0.05mm的玻璃球,球内盛有内参比溶液,为0.1mol/L HCl溶液。内参比电极为Ag/AgCl电极,插入内参比溶液。pH玻璃电极广泛用于溶液的pH测定。 -
第6题:
取20mL盐酸溶液,用0.0100mol/L的碳酸钠标准溶液标定时,恰好用了10mL碳酸钠标准溶液,则该盐酸溶液的浓度为()。
- A、0.0100mol/L
- B、0.0200mol/L
- C、0.0500mol/L
- D、0.1000mol/L
正确答案:A -
第7题:
粗纤维测定前去除碳酸盐用的试剂是()
- A、0.5mol/L盐酸溶液
- B、1.0mol/L盐酸溶液
- C、0.5mol/L硝酸溶液
- D、1.0mol/L硝酸溶液
正确答案:A -
第8题:
对于pH计电极无机盐类玷污,可在0.1mol/L的()溶液中浸泡几分钟,然后在蒸馏水中清洗。
- A、盐酸
- B、NaOH溶液
- C、酒精
- D、盐溶液
正确答案:A -
第9题:
用盐酸清洗玻璃电极上沾有的无机盐类,盐酸溶液的浓度应为()mol/L。
- A、2
- B、O.2
- C、1
- D、0.1
正确答案:D -
第10题:
用密度为1.19g/ml,质量百分浓度为38.32﹪的浓盐酸,配制10L0.1000mol/L的盐酸标准溶液,问需用上述浓盐酸多少毫升?已知:M(盐酸)=36.46g/mol
正确答案:要配制的盐酸标准溶液的摩尔数:10L×0.1000mol/L=1.000mol
已知M=36.46g/mol,
1.000×36.46=36.46g
36.46÷1.19÷38.32%=79.95ml
答:需要浓盐酸79.95毫升。 -
第11题:
pN电极受到污染后,先用()盐酸浸泡15~20min,然后用水冲洗干净,再浸泡在C.氯化钠溶液中活化。
- A、5%,0.1mol/L;
- B、10%,0.1mol/L;
- C、5%,0.01mol/L;
- D、10%,0.01mol/L。
正确答案:C -
第12题:
单选题向200mL0.1mol/L Na2SO4溶液中加入100mL0.25mol/L的Ba(OH)2溶液后,还需加入多少盐酸才能恰好完全中和( ).A10mL lmol/L盐酸
B5mL lmol/L盐酸
C50mL lmol/L盐酸
D25mL 0.5mol/L盐酸
正确答案: A解析:
Ba(OH)2溶液加入后对氢氧根离子没有消耗,所以溶液中的氢氧根离子的物质的量为为0.05mol,所以需要0.05mol的氢离子来中和. -
第13题:
被污染玻璃器皿清洗一般先用下列溶液浸泡的是
A.2%盐酸
B.肥皂水
C.2%次氯酸溶液
D.重铬酸清洗液
E.0.1mol/LNaOH
正确答案:A
-
第14题:
用微生物法测定食物中的尼克酸时,须通过水解将结合形式的烟酸转变为游离状态,用哪一种介质进行水解
A、0.1mol/L盐酸溶液
B、0.5mol/L硫酸溶液
C、pH=4.5磷酸缓冲液
D、2mol/L硫酸溶液
E、0.5mol/L盐酸溶液
参考答案:B
-
第15题:
碘酸钙中氯酸盐的检测,加入的盐酸应为( )
A.稀盐酸
B.浓盐酸
C.1 mol/L的盐酸
D.0.1 mol/L的盐酸
正确答案:B
-
第16题:
等体积混合0.1 mol/L盐酸和0.06 mol/L氢氧化钡溶液,混合后溶液的pH=____________.答案:解析:12【解题指要】
(1)设酸和碱溶液的体积均为1 L,则盐酸溶液中含HCl为0.1 mol/L×1 L=0.1 mol;
Ba(OH)2溶液中含Ba(OH)2为0.06 mol/L×l L=0.06 mol.
(2)两溶液混合时,要发生化学反应
因此,混合后可能有以下三种情况:
①恰好完全反应.因BaCl2是强酸强碱盐,所以溶液显中性.
②酸有剩余,溶液显酸性.
③碱有剩余,溶液显碱性.
究竟属于哪一种情况,需经计算才能知道.
设与盐酸完全反应需Ba(OH)2xmol,则
所以Ba(OH)2剩余:0.06 mol-0.05 mol=0.01mol.
(3)计算混合后溶液的pH.

OH一的物质的量浓度为0.005 mol/L×2=0.01mol/L,则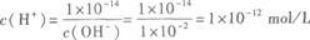
即pH=12. -
第17题:
纠正轻度代谢性碱中毒常用( )
- A、0.9%氯化钠溶液
- B、2%氯化铵溶液
- C、0.1mol/L盐酸溶液
- D、0.2mol/L盐酸溶液
- E、10%氯化钾溶液
正确答案:A -
第18题:
最常见的玻璃膜电极为pH玻璃电极,它的敏感膜是由特殊成分的玻璃制成的厚约0.05mm的玻璃球,球内盛有的内参比溶液为()
- A、1.0mol/LHCl溶液
- B、0.02mol/LHCl溶液
- C、0.1mol/LNHCl溶液
- D、0.2mol/LHCl溶液
- E、0.1mol/LHCl溶液
正确答案:E -
第19题:
碘酸钙中氯酸盐的检测,加入的盐酸应为()
- A、稀盐酸
- B、浓盐酸
- C、1mol/L的盐酸
- D、0.1mol/L的盐酸
正确答案:B -
第20题:
在200毫升稀盐酸溶液中,含有0.73克氯化氢,则溶液的物质的量浓度为()。
- A、0.01mol/L
- B、0.1mol/L
- C、0.01L/mol
- D、0.1L/mol
正确答案:B -
第21题:
用标准的盐酸溶液来滴定待测NaOH溶液,已知盐酸溶液物质的量浓度为0.02mol/L,用量为20mL,待测NaOH溶液的用量为40mL,则NaOH溶液物质的量浓度为()。
- A、0.01mol/L
- B、0.02mol/L
- C、0.03mol/L
- D、0.05mol/L
正确答案:A -
第22题:
用酸度计测酸时,对玻璃电极初次使用,一定要先在()中浸泡24小时以上。
- A、蒸馏水
- B、1mol/l盐酸溶液
- C、1mol/l氢氧化钠溶液
- D、1mol/l氯化钠溶液
正确答案:A -
第23题:
填空题0.1mol/L的盐酸溶液的 pH值为()。正确答案: 1解析: 暂无解析
