一定条件下,可逆反应:3A(g)+2B(g)2C(g)达到平衡的标志是()。A、C生成的速率与C分解的速率相等B、C的浓度不再变化C、单位时间生成3molA,同时生成2molBD、D.B.C的分子数之比为3:2:2
题目
一定条件下,可逆反应:3A(g)+2B(g)2C(g)达到平衡的标志是()。
- A、C生成的速率与C分解的速率相等
- B、C的浓度不再变化
- C、单位时间生成3molA,同时生成2molB
- D、D.B.C的分子数之比为3:2:2
相似考题
参考答案和解析
更多“一定条件下,可逆反应:3A(g)+2B(g)2C(g)达到平衡的标志是()。A、C生成的速率与C分解的速率相等B、C的浓度不再变化C、单位时间生成3molA,同时生成2molBD、D.B.C的分子数之比为3:2:2”相关问题
-
第1题:
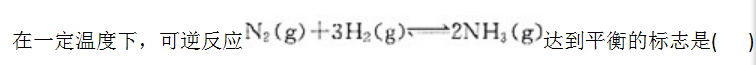 A.NH3(g)生成的速率与分解的速率相等
A.NH3(g)生成的速率与分解的速率相等
B.单位时间内生成nmolN2,同时生成nmolH2
C.反应已经停止
D.生成物的分压等于反应物的分压答案:A解析:平衡状态是动态的平衡 -
第2题:
某一温度时,当反应2SO2(g)+O2(g)←→2SO3(g)达到平衡时,是指()
- A、SO2不再发生反应
- B、2molSO2和1molO2反应,生成2molSO3
- C、SO2、O2、SO3浓度相等
- D、SO2和O2生成SO3的速度等于SO3分解的速度
正确答案:D -
第3题:
当可逆反应达到平衡时,各反应物和生成物的浓度一定相等。
正确答案:错误 -
第4题:
当可逆反应达到平衡时,各反应和生成物的浓度一定相等。
正确答案:错误 -
第5题:
在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)2Z(g)此反应达到平衡的标志是()。
- A、容器内压强不随时间变化
- B、容器内各物质的浓度不随时间变化
- C、容器内X、Y、Z的浓度之比为1:2:2
- D、单位时间消耗0.1molX同时生成0.2molZ
正确答案:A,B -
第6题:
可逆反应,C(s)+H2O→CO(g)+H2(g)ΔH>0,下列说法正确的是()
- A、达到平衡时,反应物的浓度和生成物的浓度相等;
- B、达到平衡时,反应物和生成物的浓度不随时间的变化而变化;
- C、由于反应前后分子数相等,所以增加压力对平衡没有影响
- D、升高温度使正反应速度增大,逆反应速度减小,结果平衡向右移
正确答案:B -
第7题:
可逆反应当()与()相等时,可逆反应达到平衡。
- A、正反应速率
- B、逆反应速率
- C、反应物浓度
- D、生成物浓度
正确答案:A,B -
第8题:
对于任何一个可逆反应,下列说法正确的是()
- A、达平衡时反应物和生成物的浓度不发生变化
- B、达平衡时正反应速率等于逆反应速率
- C、达平衡时反应物和生成物的分压相等
- D、达平衡时反应自然停止
正确答案:A,B -
第9题:
在一定条件下,一个反应达到平衡的标志是()。
- A、各反应物和生成物的浓度相等
- B、各物质浓度不随时间改变而改变
- C、 △rGm = 0
- D、正逆反应速率常数相等
正确答案:B -
第10题:
某温度下,化学反应2NO(g)+O2(g)=2NO2(g)达平衡,下列说法中正确的()。
- A、反应物已消耗完
- B、不再有产物生成
- C、正逆反应速率相等
- D、反应已停止
正确答案:C -
第11题:
在一定温度下H2(气)+I2(气)=2HI(气)达到平衡的标志是()。
- A、单位时间内生成n moLH2,同时生成n mol12
- B、容器内总压强不随时间而变化
- C、单位时间内生成2n moLHI,同时生成n moLH2
- D、单位时间内生成2n moLHI,同时生成2n moLH2
正确答案:C -
第12题:
单选题某温度下,化学反应2NO(g)+O2(g)=2NO2(g)达平衡,下列说法中正确的()A反应物已消耗完
B不再有产物生成
C正逆反应速率相等
D反应已停止
正确答案: A解析: 暂无解析 -
第13题:
可逆反应C(s)+H2O⇄CO(g)+H2(g)△H>0,下列说法正确的是()
- A、达到平衡时,反应物的浓度和生成物的浓度相等
- B、达到平衡时,反应物和生成物的浓度不随时间的变化而变化
- C、由于反应前后分子数相等,所以增加压力对平衡没有影响
- D、升高温度使V正增大,V逆减小,结果平衡向右移动
正确答案:B -
第14题:
某一温度时,当反应 2SO2(g)+ O2(g)←→2SO3(g)达平衡时,是指()。
- A、SO2不再发生反应
- B、2molSO2和1molO2反应,生成2molSO3
- C、SO2,O2,SO3浓度相等
- D、SO2和O2生成SO3的速度等于SO3分解的速度
正确答案:D -
第15题:
可逆反应,C(s)+H2OCO(g)+H2(g)△H>0,下列说法正确的是()
- A、达到平衡时,反应物的浓度和生成物的浓度相等
- B、达到平衡时,反应物和生成物的浓度不随时间的变化而变化
- C、由于反应前后分子数相等,所以增加压力对平衡没有影响
- D、加入正催化剂可以加快反应达到平衡的速度
- E、升高温度使V正增大,V逆减小,结果平衡向右移动
正确答案:B,D -
第16题:
化学反应达到平衡的特征是()
- A、各反应物和生成物的浓度相等
- B、正逆反应物的速率常数相等
- C、各反应物和生成物的浓度等于常数
- D、各物质的浓度不随时间而变
正确答案:D -
第17题:
反应2A((g)=2B(g)+E(g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是()。
- A、加压;
- B、减压;
- C、减小E的浓度;
- D、降温
正确答案:D -
第18题:
在一定温度下,可逆反应A(g)+3B(g)⇌2C(g)达到平衡的标志是()。
- A、C的生成速率与C的分解速率相等
- B、单位时间内生成n摩尔A同时生成3n摩尔B
- C、ABC浓度不再发生变化
- D、ABC的物质的量的浓度为1:3:2
正确答案:A,C -
第19题:
在一定温度下,可逆反应A(g)+3B(g)2C(g)达到平衡的标志是()。
- A、C生成的速率和C分解的速率相等
- B、单位时间生成nmolA,同时生成3molB
- C、A、B、C的分子数比为1:3:2
- D、C生成的速率为0
正确答案:A -
第20题:
在一定温度下,可逆反应A(g)+3B(g)=2C(g)达到平衡的标志是()。
- A、C的生成速率与C的分解速度相等
- B、单位时间内生成n molA同时生成3n molB
- C、A、B、C浓度不再发生变化
- D、A、B、C的物质的量之比为1:3:2
正确答案:A,C -
第21题:
下列与化学反应能量变化相关的叙述正确的是()。
- A、生成物总能量一定低于反应物总能量
- B、放热反应的反应速率总是大于吸热反应的反应速率
- C、应用盖斯定律,可计算某些难以直接测量的反应焓变
- D、同温同压下,H2>(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
正确答案:C -
第22题:
反应A+2D→3G在298K于2dm3容器中进行,若某时刻反应进度随时间变化率为0.3mol·s-1,则此时A的消耗速率为();G的生成速率为()。
正确答案:0.15mol·dm-3·s-1;0.45 mol·dm-3·s-1 -
第23题:
填空题对于可逆反应2SO2(g)+O2(g)2SO3(g)+Q,当达到平衡后,若升高温度,正反应速率____,逆反应速率____(选填加快、减慢或不变),平衡____移动(选填向右、向左或不).正确答案: 加快,加快,向左解析:
(1)根据温度对反应速率的影响可知,温度升高,反应速率加快,所以正反应速率和逆反应速率都加快;(2)根据平衡移动原理可知,升高温度,平衡向吸热方向移动.对此反应来说,即向左移动;从反应速率角度看,虽然v正、v逆都增大,但增大的倍数是不同的.对此反应的结果是v正<v逆,所以平衡要向左移动.
